RESEÑA
BIBLIOGRÁFICA
El
níquel en suelos y plantas de Cuba
Nickel
in soils and plants of Cuba
Dr.C.
Olegario Muñiz Ugarte,I M.Cs. Mirelys Rodríguez Alfaro,I
M.Cs. Alfredo Montero Álvarez,II Dr.C. Juan Estévez
Álvarez,II Dra.C. Adriana M. de Aguiar Accioly,III
Clístenes W. Araujo Do NascimentoIV
IInstituto
de Suelos, Autopista Costa-Costa, km 8½, Apdo. 8022, CP 10 800, Capdevila,
Boyeros, La Habana.
IICentro de Aplicaciones Tecnológicas y Desarrollo Nuclear,
La Habana.
IIIEMBRAPA. Mandioca y Fruticultura Tropical, Cruz Das
Almas, Bahía, Brasil.
IVUniversidad Federal Rural de Pernambuco, Recife, Pernambuco, Brasil.
RESUMEN
El contenido de
Níquel (Ni) en el suelo es muy dependiente del material parental que
le dio origen. Por otra parte, el Ni existente en su superficie, puede ser también
un reflejo de su contaminación. La literatura internacional señala
valores de Ni total en los suelos del mundo entre 0,2 y 450 mg kg-1.
Se conoce en la actualidad, que aunque el Ni es esencial para las plantas superiores,
su exceso en forma disponible puede ser tóxico, por lo que se considera
un Metal Pesado. En Cuba las encuestas realizadas reflejan un contenido medio
de 122,3 mg kg-1 de Ni total, muy superior al señalado por
la literatura internacional y valores extremos de hasta 2850,0 mg kg-1
en suelos desarrollados sobre rocas ultrabásicas (serpentinita). Sin
embargo, no existen reportes de valores elevados (tóxicos) del elemento
en los cultivos. En el trabajo se discute el origen y formas en que se encuentra
el Ni en los suelos cubanos; así como su posible efecto tóxico
para las plantas y animales que se alimentan de ellas. Finalmente, se concluyó
planteando la necesidad de establecer Límites Permisibles de Ni en el
suelo, diferenciados de acuerdo al tipo de suelo y su uso.
Palabras
clave: contaminación, metales pesados, suelo.
ABSTRACT
Soil Nickel (Ni)
content is very dependant of the parental material that originated it. Besides,
Ni in the soil surface could reveal also its contamination. The international
bibliography shows total Ni values in soils of the world between 0,2 and 450
mg kg-1. At present it is known that despite Ni is essential for
higher plants, an excess in available forms could be toxic and it is considered
a Heavy Metal. In Cuba, studies indicate a total Ni mean content of 122,3 mg
kg-1, much higher than the one pointed out by the bibliography and
extreme values up to 2850,0 mg kg-1 in soils developed over ultrabasic
rock (serpentinite). Nevertheless, there are no reports of high values (toxic)
in crops. In present paper, it is discussed the origin and forms of Ni in Cuban
soils, and its possible toxic effect for plants and animals that feed with them.
Finally, it was concluded that it is necessary to establish Permissible Limits
of Ni in soils, according to the soil type and use.
Key words:
pollution, heavy metals, soil.
INTRODUCCIÓN
El Níquel
(Ni) como elemento químico, tiene número atómico 28; masa
atómica 58,69; densidad 8,20 g cm-3 y su principal estado
de oxidación es +2. El Ni pertenece a la familia del Hierro (Fe), que
incluye al Cobalto (Co), ambos de característica geológica del
tipo siderofílica, por lo que se combina fácilmente con el Fe
metálico. Además, forma con facilidad compuestos de sulfuro y
sulfo arseniuros (1). La abundancia media del Ni en la corteza terrestre se
estima en alrededor de 20 mg kg-1, mientras que en las rocas ultrabásicas
(ultramáficas) como es el caso de la serpentinita, varía entre
1 400 y 2 000 mg kg-1 y su concentración disminuye con el
incremento de la acidez de la roca; en el granito contiene entre 5 y 20 mg kg-1.
Las rocas sedimentarias contienen el Ni en el rango entre 5 y 90 mg kg-1,
con el mayor valor en los sedimentos arcillosos (1, 2, 3, 4).
El primer artículo conocido sobre la importancia del Ni, Cr y Co data
del año 1935 (5) cuando se estudiaron los suelos ultrabásicos
de Cuba, Puerto Rico y Estados Unidos, con el fin de explicar su infertilidad
sobre la base de los altos contenidos de estos metales en dichos suelos. Sin
embargo, hoy se conoce, que esto es debido más a los altos contenidos
de Mg, mayores que los de Ca. Más aun, los contenidos de esos metales
en las plantas que crecieron en los mismos, son menores a los encontrados en
otros lugares (6).
Las rocas ultrabásicas (ultramáficas) son rocas ígneas
constituidas esencialmente por minerales ferromagnesianos. En la parte oriental
de Cuba existen áreas significativas de suelos desarrollados sobre este
tipo de roca (5). Los afloramientos de rocas ultramáficas (serpentinas)
de Cuba son los más extensos del Caribe, abarcando aproximadamente el
7 % de la superficie total del país (7).
El contenido total de Ni en el suelo es altamente dependiente de su contenido
en el material parental (roca formadora) del mismo. No obstante, la concentración
del Ni en su superficie, puede reflejar el impacto tanto del proceso de formación
del suelo como de la contaminación (1, 3, 8, 9). Se reporta que el Ni
total en los suelos del mundo varía entre 0,2 y 450 mg kg–1
y su contenido medio entre 19 y 22 mg kg–1 (1); pero otros autores
señalan que éste último se encuentra entre 20 y 40 mg kg–1
(8).
Se conoce en la actualidad, que aunque el Ni es esencial para las plantas superiores,
como cofactor de la enzima ureasa y por su efecto en la nodulación de
las leguminosas y en la nitrificación y mineralización del N;
su exceso en forma disponible a las plantas puede ser tóxico (1, 2, 3,
8), de ahí que sea considerado como Metal Pesado (MP). Las investigaciones
indican que los efectos de la toxicidad del Ni en el hombre, son neurológicos,
reproductivos y carcinogénicos (10, 11). Se deben tomar particulares
cuidados en la industria del Ni, ya que es sumamente tóxico cuando se
inhala. De tal forma que los procesos industriales en que se utiliza este metal,
así como el carbón y el petróleo, se consideran fuentes
contaminantes (1, 3, 12).
El presente trabajo, se propone reseñar de forma coherente y cronológica,
la información emanada de diferentes trabajos y proyectos realizados
en Cuba acerca del origen, contenido y formas del Ni en los suelos cubanos;
así como, su posible efecto tóxico en las plantas y como consecuencia
en el hombre. Resulta conveniente aclarar, que al nombrar los tipos de suelos,
se empleó la Clasificación Cubana existente en el momento que
se realizó el trabajo. No obstante, existen correlaciones con las otras
Clasificaciones Nacionales previas o posteriores y con las internacionales (13,
14).
MÉTODOS
ANALÍTICOS EMPLEADOS
Se estudió
el contenido de Ni total o semi total en el suelo, por ser las formas usualmente
empleadas para evaluar contaminación del suelo por MP. En el tiempo,
el método utilizado para la mineralización de la muestra ha ido
cambiando, lo cual se aclara en cada caso particular. En todos los casos se
empleó la espectrofotometría de absorción atómica
con llama o la de plasma acoplada (ICP) como técnica analítica
instrumental (12, 15, 16).
EL Ni
EN LOS SUELOS DE CUBA
Existe una tesis
de doctorado realizada en la desaparecida Unión Soviética, no
publicada, en la cual se estudiaron microelementos, entre ellos el Ni, en perfiles
de suelos cubanos cultivados con caña de azúcarA.
Pocos años después, se realizó una encuesta sobre el contenido
de algunos MP en los suelos (17, 18). Las determinaciones se realizaron durante
1987 en colaboración con el IPE JENA de la desaparecida República
Democrática Alemana (RDA). Se utilizaron 85 muestras de suelo provenientes
de la capa arable de perfiles típicos de 10 provincias del país
y el municipio especial Isla de la Juventud, las que fueron procesadas mediante
extracción con HNO3 1,5 N (18). Los resultados (Tabla
I) reflejaron un contenido medio de 122,3 mg kg-1 de Ni total,
y valores extremos de hasta 2850,0 mg kg-1, muy superior a los señalados
por la literatura internacional de la época (1, 8); los cuales correspondieron
principalmente a los suelos Fersialítico Rojo Pardusco Ferromagnesial,
desarrollados sobre serpentinita (13, 14), de la provincia de Holguín,
donde existen grandes yacimientos niquelíferos.

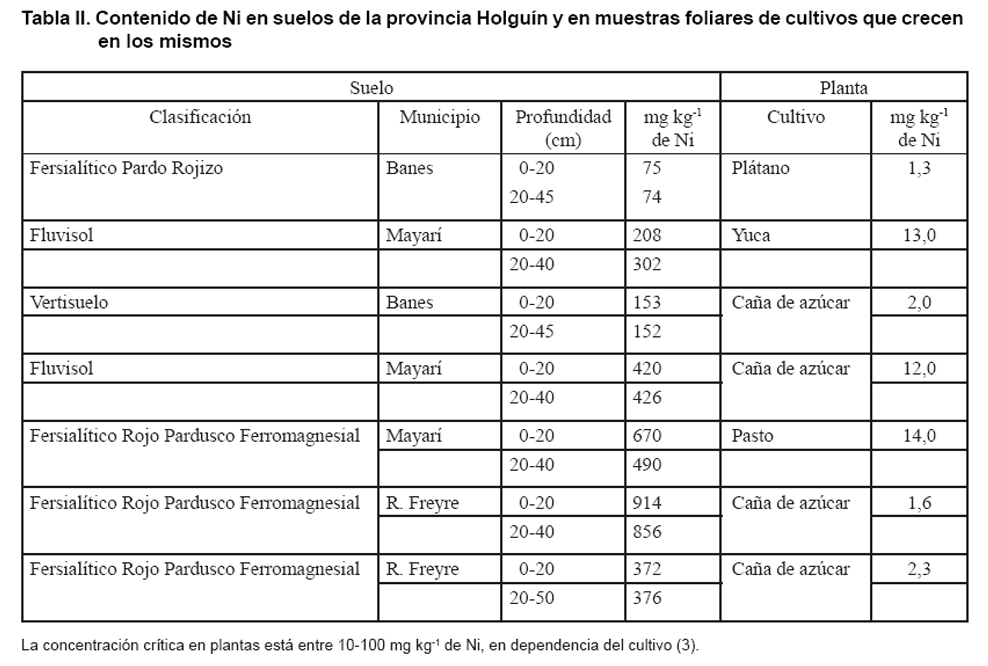
No obstante, en el mismo trabajo se tomaron muestras foliares de los cultivos
que crecían en algunos de los suelos estudiados de Holguín, y
en todos los casos los contenidos de Ni, fueron adecuados (Tabla
II), por lo que los autores concluyeron que los mismos provienen del material
parental que dio origen al suelo (litogénico) y se encuentran, en su
mayor extensión, en formas no disponibles a las plantas.
Además, se encontró que los suelos Ferralítico Rojo (13,
14), de particular importancia agrícola en las actuales provincias de
Mayabeque, Artemisa, Matanzas y Ciego de Ávila, desarrollados sobre rocas
sedimentarias calizas, poseen contenidos totales de Ni altos, en el entorno
de los 200 mg kg-1, aunque no tan elevados como los anteriores, sí
son superiores a los reportados en la literatura internacional de la época.
De igual forma, se encontró que la mayor parte del Ni estaba en forma
no disponible a las plantas, por lo que se concluyó que su origen también
es litogénico (17, 18). Estos suelos se caracterizan por la formación
de minerales arcillosos del tipo 1:1 y acumulación de óxidos e
hidróxidos de Fe y Al. El Ni del suelo está fuertemente asociado
con los óxidos de Fe y Mn (1). Los óxidos de Fe y los minerales
contienen Ni en el rango entre 100 y 170 mg kg-1, mientras que las
concreciones de Fe-Mn acumulan hasta 680 mg kg-1 (1, 9). Téngase
en cuenta, que alrededor del 70 % de los suelos cubanos, están desarrollados
sobre rocas sedimentarias calizas y se plantea que las mismas en su formación
se enriquecieron en Ni y Cr proveniente de las zonas ricas en rocas ultrabásicas
(19, 20, 21).
Posteriormente, se corroboró lo antes planteadoB
y se demostró que las adiciones de elevadas cantidades de Ni en forma
asimilable, a los dos tipos de suelos (Fersialítico Rojo Pardusco Ferromagnesial
y Ferralítico Rojo), son fijadas rápidamente en el mismo y no
asimiladas por la planta, por lo que los altos contenidos totales de Ni no constituyen
causa de contaminación en los cultivos que crecen en ellos (9).
En otros trabajos, se estudió la determinación de las llamadas
formas disponibles con diferentes soluciones extractivas (1, 4, 6), la más
empleada, el DTPA (22). No obstante, los resultados no han permitido arribar
a resultados concluyentes (1, 2, 3, 6).
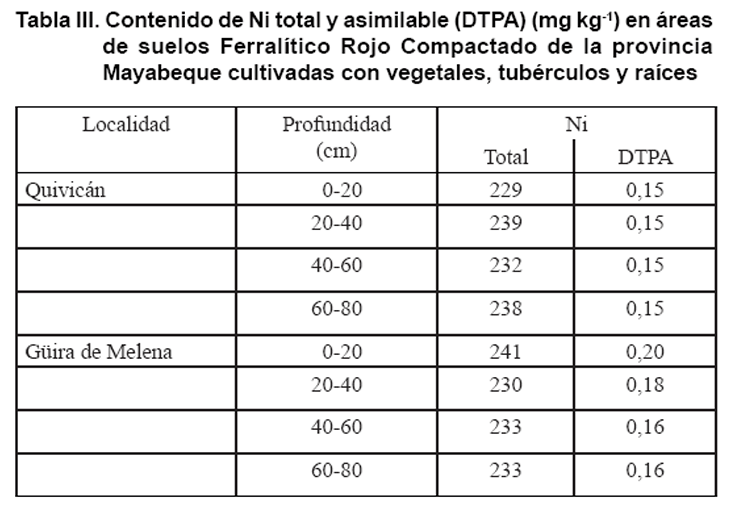
La Tabla III muestra
que aunque con frecuencia se plantea la mayor acumulación de los MP en
la capa arable del suelo, resulta evidente la distribución uniforme del
Ni total a lo largo del perfil de suelo, lo que ratifica el carácter
litológico del mismo. Obsérvese además, que la fracción
disponible o asimilable, resulta una muy pequeña fracción del
total, lo que coincide con los bajos contenidos de Ni foliares obtenidos en
diferentes estudiosC
(23, 24).
Existen otros tipos de suelos cubanos, que con frecuencia presentan contenidos
de Ni total entre 100 y 200 mg kg–1, este es el caso de los Ferríticos,
Vertisoles, Fluvisoles y muchos Pardo Sialíticos; sin embargo, los de
textura arenosa de Pinar del Río y la Isla de la Juventud usualmente
tienen bajos o muy bajos contenidos de este metalD
(17).
FITOTOXICIDAD
DEL Ni EN TRES SUELOS CUBANOS
En otro proyectoD,
durante la segunda parte de los años 90, se estudió en tres tipos
de suelos cubanos, Ferralítico Rojo, Alítico de Baja Actividad
Arcillosa (ABAA) y Vertisol Pélico (13, 14), la adición de dosis
crecientes de Ni (0, 100, 200, 400 y 800 mg kg-1) en la forma de
sal soluble, utilizando macetas plásticas conteniendo 1 kg de suelo,
con el fin de provocar toxicidad en plantas crecidas en esos suelos. Una vez
adicionado el Ni, se dejó la maceta en reposo durante 30 días
y se sembró sorgo (seis plantas por maceta) el que se cosechó
a los 45 días de germinado. Se evaluó el rendimiento (como materia
seca producida), el contenido del metal pesado en los cultivos y por cálculo,
la extracción correspondiente del mismo, con el fin de evaluar la Fitotoxicidad
del Ni, para lo cual se definió el Nivel Crítico de Fitotoxicidad
en el suelo, como aquél que dio lugar a una disminución estadísticamente
significativa del rendimiento.
En el caso del suelo Ferralítico Rojo (13, 14), la aplicación
de hasta 800 mg kg-1 de Ni al suelo, dio lugar a un tenor en el mismo
de 1131,8 mg kg-1 de Ni total, pero no afectó de forma significativa
el rendimiento del cultivo considerado, ni dio lugar a síntomas visuales
en las plantas. Además, los contenidos en planta fueron inferiores a
30 mg kg-1, valor considerado como Criterio de Fitotoxicidad en planta
para este elemento metálico (25). Lo que permite inferir que este tipo
de suelo, se caracteriza por poseer minerales del tipo 1:1 e hidróxidos
de hierro y aluminio con una elevada capacidad de fijación de este metal.
Sin embargo, en el caso del suelo de textura arenosa Alítico de Baja
Actividad Arcillosa (ABAA) (13, 14), por sus características químicas
y físicas, mantienen en forma disponible a las plantas una mayor proporción
del Ni aplicado, que el suelo Ferralítico Rojo, por lo que la planta
lo absorbe en mayor proporción. De tal forma que se obtuvo una caída
significativa del rendimiento para un contenido de Ni total en el suelo de 407
mg kg-1, tenor al que correspondió un contenido en planta
de 49,30 mg kg-1 de Ni, superior a los 30 mg kg-1 considerado
como fitotóxico (25).
Por último, en el caso del Vertisol Pélico, la disminución
significativa del rendimiento se obtuvo para un tenor total de Ni en el suelo
de 451 mg kg-1, al cual correspondió un contenido en planta
también superior al fitotóxico anteriormente mencionado. Los resultados
se resumen en la Tabla
IV.

Se reporta que el síntoma visual más común de la fitotoxicidad
por Ni es la clorosis seguida por el amarillamiento y la necrosis de las hojas.
Lo cual está inducido principalmente por la interacción Fe-Ni,
es decir, baja concentración foliar de Fe debida a concentraciones elevadas
de Ni en el medio (3). No obstante, estos síntomas no se observaron en
los experimentos anteriores.
DISTRIBUCIÓN DELl Ni EN PLANTA
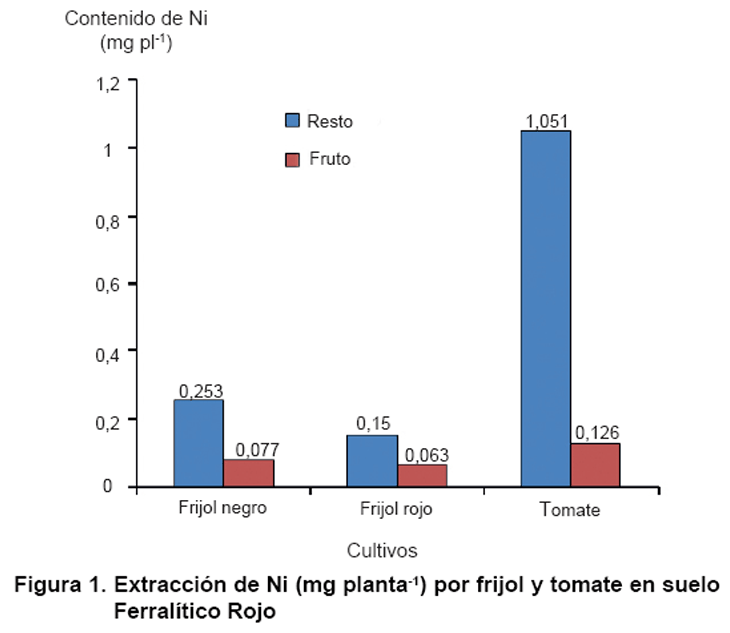
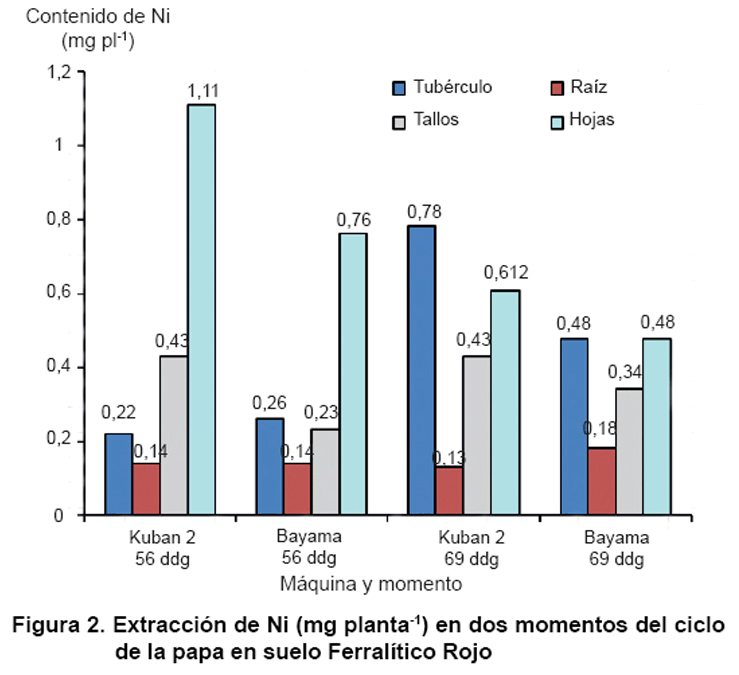
Se estudió
la extracción de Ni por órganos de la planta en los cultivos frijol,
tomate, papa y tabaco crecidos sobre suelo Ferralítico Rojo Compactado
en áreas de agricultura intensiva; así como pimiento, melón
y col en casas de cultivo, todos de las provincias Mayabeque y Artemisa. Algunos
resultados se muestran en las Figuras
1 y 2. De forma
general, los resultados indican que los contenidos de Ni en los órganos
comestibles de los cultivos estudiados no constituyen un riesgo para la salud
humana, ya que la mayor parte del metal no es traslocado al frutoC
(23, 24).
No obstante, debe aclararse que, a diferencia de lo que ocurre para MP como
el Arsénico (As), Cadmio (Cd), Plomo (Pb) y Mercurio (Hg), el Codex Alimentario
no establece límites permisibles para el Ni en los alimentos frescos
o en conserva (26).
Las formas del Ni en el suelo son diversas y van desde las muy móviles
hasta las no reactivas (4, 12, 27). El contenido de Ni en las plantas es muy
dependiente de su origen y de las propiedades del suelo, que como el contenido
de arcilla, de materia orgánica y el pH, controlan el comportamiento
del Ni y su disponibilidad a las plantas (1, 3, 9). En los cereales varía
entre 0,34 y 14,6 mg kg-1 y los valores medios, en dependencia del
cultivo, usualmente no sobrepasan 1,28 mg kg-1 (3).
Existen además metodologías que permiten la extracción
secuencial (fraccionamiento) de los MP en el suelo. De forma general, todas
comienzan con la extracción de la fracción soluble en agua, y
le siguen la intercambiable, la adsorbida u ocluida en carbonatos, y las ocluidas
en la materia orgánica, óxidos de Mn, óxidos amorfos y
cristalinos de Fe y finalmente, la residual (28, 29, 30, 31). Resulta lógico
que las formas predominantes en cada caso, dependerán del equilibrio
que exista entre factores como el pH, mineralogía, tenor y tipo de humus.
Los resultados obtenidos al profundizar en las formas en que se encuentra el
Ni en los suelos Ferralítico Rojo y Gley Ferralítico de La Habana
y Pinar del Río, respectivamente, indican que la mayor parte del mismo
se encuentra en formas no asimilables por las plantas (24).
Por otra parte, se reporta un gran número de plantas (317 Taxas y 37
Familias) catalogadas como acumuladoras e hiperacumuladoras de Ni que pueden
extraer 10 000 mg kg-1 de Ni o más. Las más conocidas
son las Alyssum sps.
Estas especies pueden extraer hasta 400 kg de Ni de una hectárea. El
mecanismo de la hiperacumulación del Ni por las plantas no es bien conocido,
pero se considera asociado a los complejos órgano-metálicos que
transportan el metal dentro de la planta (7, 32, 33, 34). Estas plantas son
características de los suelos desarrollados sobre serpentinita. Cuba
posee los afloramientos de rocas ultramáficas (serpentinas) más
extensos del Caribe, abarcando aproximadamente 5 300 km² que representan
el 7 % de la superficie total del país, siendo el país de las
Antillas que mayor número de especies hiperacumuladoras posee (35, 36,
37).
Una de las alternativas para remediar las áreas contaminadas es la extracción
de los metales pesados por las plantas hiperacumuladoras. Esta técnica
es conocida como Fitorremediación, Fitoextracción o Biorremediación,
técnica que involucra a plantas y microorganismos en el saneamiento ambiental
(12, 38, 39, 40, 41).
EL
Ni EN LOS ABONOS ORGÁNICOS
En Cuba, la desaparición
del campo socialista europeo dio lugar a la abrupta disminución en el
consumo de los fertilizantes minerales y otros insumos con el consiguiente efecto
negativo en la producción agrícola. Sin embargo, el empleo de
las diferentes fuentes de abonos orgánicos (AO) ha resultado una alternativa
para la recuperación de la producción agrícola (42, 43).
En ocasiones se considera que todo AO es adecuado, pero no es así. Se
requiere la previa evaluación de su calidad, lo que incluye el posible
contenido de patógenos y de MP. Esto reviste mayor importancia, al considerar
las fuertes cargas de AO que sustentan la Agricultura Urbana y en especial los
Organopónicos. De tal forma que durante los últimos 10 años,
se realizaron estudios que incluyeron el monitoreo de los MP en las diferentes
fuentes orgánicas (44).
En el caso del Ni, los valores obtenidos son usualmente mayores a los reflejados
en la literatura internacional, de forma análoga a lo ocurrido en las
muestras de suelo; lo que indica la influencia del suelo en el sistema suelo-planta-animal:
a contenidos altos de Ni en el suelo, corresponden usualmente, contenidos también
altos en los diferentes AO producidos. No obstante los tenores de Ni en los
cultivos crecidos con el uso de los mismos, son bajos, lo que denota una vez
más, que el mismo se encuentra en forma no asimilable por las plantas.
Algo similar ocurre con los sustratos que se emplean en los Organopónicos,
que se obtienen a partir de los AO (44).
El Ministerio de Agricultura, Pecuaria y Abastecimiento de Brasil fija como
Límite Máximo Permisible de los fertilizantes orgánicos
para su uso agrícola 70 mg kg-1 de Ni como peso seco. En Cuba
se trabaja actualmente con este fin.
Como fue discutido, el Ni en el suelo es poco móvil y se encuentra principalmente
en su fracción residual. Existe evidencia de que en el horizonte superficial,
el Ni puede estar fuertemente ligado a la forma orgánica y por tanto,
es poco móvil. No obstante, su removilización parece posible mediante
la presencia de ácidos húmicos y fúlvicos (1).
ESTUDIOS
EN DESARROLLO
Se trabaja actualmente,
con la colaboración y experiencia de instituciones brasileñas,
en el desarrollo de investigaciones que posibilitarán elaborar una Legislación
contentiva de los Límites Permisibles de Metales Pesados, inclusive el
Ni, en los suelos de Cuba, basada en metodologías internacionales que
incluyen el empleo de la modelación y el Análisis de Riesgo (45,
46).
CONCLUSIONES
Y
RECOMENDACIONES GENERALES
Muchos suelos
cubanos se caracterizan por altos valores de Ni total. Sin embargo, no existe
evidencia de la existencia de contenidos tóxicos (para el hombre) o fitotóxicos,
en los cultivos que en ellos crecen, ya que en el suelo la mayor parte del Ni
se encuentra en formas no disponibles a las plantas. Los valores más
elevados son característicos de los suelos Fersialítico Rojo Pardusco
Ferromagnesial (más de 2 000 mg kg-1), desarrollados sobre
roca serpentinita, suelos poco productivos debido, más que al elevado
tenor de Ni, a la inversa relación Mg/Ca, entre otros factores limitantes.
La industria del Ni constituye la principal fuente de contaminación de
los suelos en este metal. Como quiera que la misma es de primordial importancia
para la economía cubana, se deben tomar particulares cuidados, ya que
el Ni es sumamente tóxico cuando se inhala.
Otros suelos de gran importancia agrícola, como los Ferralítico
Rojo, abundantes en la llanura Habana-Matanzas y en Ciego de Ávila, también
tienen altos contenidos de Ni, aunque con valores no tan elevados (100 y 200
mg kg–1). Los suelos Ferríticos, Vertisoles, Fluvisoles y
muchos Pardo Sialíticos, con frecuencia presentan valores en este rango.
Aunque las investigaciones realizadas indican que en los cultivos de importancia
económica, los contenidos de Ni en la parte comestible de los mismos
son bajos, resulta conveniente estudiar el posible efecto de propiedades del
suelo, como el pH y el contenido de materia orgánica y de arcilla, sobre
el incremento de las formas disponibles a las plantas. En este sentido, la extracción
secuencial (fraccionamiento) de las diferentes formas existentes en el suelo,
arrojará nuevos elementos.
Los contenidos de Ni en las fuentes orgánicas que se emplean como abono,
resultan superiores a los reportados por muchos países, en lo que sin
lugar a dudas incide, los correspondientes elevados valores en los suelos, pero
tampoco se han detectado efectos tóxicos del mismo en el hombre. No obstante,
debe tenerse en cuenta que el Ni, no es de los elementos regulados por el Codex
Alimentario, por lo que no existe criterio internacional al respecto. Sin embargo,
resulta imprescindible que se mantenga el monitoreo del contenido de los MP
(no solo del Ni) en todas las fuentes orgánicas en uso. De igual forma,
resulta aconsejable continuar estudios sobre las potencialidades de la Fitoextracción
o Fitorremediación como técnica promisoria para el saneamiento
y recuperación de suelos contaminados por metales como el Ni.
Finalmente, se recomienda profundizar en las investigaciones con este y el resto
de los MP, con el fin de lograr una primera versión de Legislación
cubana sobre Límites Permisibles de Metales Pesados en los suelos cubanos.
Notas al
pie
A
Companioni, N. Formas de los compuestos de los microelementos en los suelos
de las plantaciones de caña de la República de Cuba. [Tesis de
Doctorado], Moscú, URSS, 1981, 110 p.
B
Irigoyen, H. y Muñiz, O. Contenido de Ni, Cr, Cd, Pb, Cu y Zn en suelos
Ferralítico Rojo y Fersialítico Rojo Parduzco Ferromagnesial cubanos.
edit. Archivos del Instituto de Suelos, La Habana, 1989, 15 p.
C
Muñiz, O. Contenido de metales pesados en áreas de agricultura
intensiva de La Habana y Pinar del Río. Informe Final del Proyecto 07
perteneciente al PR-11: Recursos Naturales, Inst. Archivos del Instituto de
Suelos, La Habana, Cuba, 2004, 37 p.
D
Muñiz, O.; Molina, J.; Estévez, J.; Quicute, S.; Vega, E.; Montero,
A.; Pupo, I. y Padilla, R. Contaminación por metales pesados en algunos
de los principales agroecosistemas cubanos. Informe Final del Proyecto 002.042
perteneciente al PNCT Producción de Alimentos por Métodos Sostenibles,
Inst. Archivos del CITMA, La Habana, Cuba, 2000, 25 p.
BIBLIOGRAFÍA
1. Kabata-Pendias,
A. y Mukherjee, A. B. Trace Elements from Soil to Human [en línea]. edit.
Springer Berlin Heidelberg, 2007, 519 p., ISBN 978-3-540-32713-4, DOI http://dx.doi.org/10.1007/978-3-540-32714-1,
[Consultado: 28 de noviembre de 2015], Disponible en: <http://link.springer.com/pter/10.1007/978-3-540-32714-1_1>.
2. Alloway, B. J. ‘‘The Origin of Heavy Metals in Soils’’. En: Heavy Metals
in Soils, edit. Springer Science & Business Media, 1995, pp. 38-57, ISBN
978-0-7514-0198-1, DOI http://dx.doi.org/10.1007/978-94-011-1344-1_3.
3. Kabata-Pendias, A. Trace Elements in Soils and Plants [en línea].
4.a ed., edit. CRC Press, 2010, 407 p., ISBN 978-1-4200-9368-1, DOI http://dx.doi.org/10.1201/b10158,
[Consultado: 28 de noviembre de 2015], Disponible en: <http://www.crcnetbase.com/doi/book/10.1201/b10158>.
4. Alloway, B. J. Heavy Metals in Soils [en línea]. (ed. Alloway B. J.),
(ser. Environmental Pollution, no. ser. 22), 3.a ed., edit. Springer Netherlands,
2013, 613 p., ISBN 978-94-007-4469-1, DOI http://dx.doi.org/10.1007/978-94-007-4470-7,
[Consultado: 28 de noviembre de 2015], Disponible en: <http://link.springer.com/pter/10.1007/978-94-007-4470-7_1>.
5. Robinson, W. O. y Edgington, H. G. ‘‘Chemical studies of infertile soils
derived from rocks high in Magnesium and generally high in Chromium and Nickel’’.
Technical Bulletin of the United States Department of Agriculture,
no. 471, 1935, pp. 1-29.
6. Proctor, J. y Baker, A. J. M. The importance of nickel for plant growth in
ultramafic (Serpentine) soils. [en línea]. (ed. Ross S. M.), 1.a ed.,
edit. John Wiley & Sons Ltd, 1994, ISBN 978-0-471-94279-5, [Consultado: 28
de noviembre de 2015], Disponible en: <http://www.cabdirect.org/abstracts/19940706052.html>.
7. Glaría, A. V.; González-Torres, L. R.; Iturralde, R. B. y Granados,
E. B. ‘‘Flora de la región ultramáfica (serpentinícola)
de Guamuhaya’’. Revista del Jardín Botánico Nacional,
vol. 27-28, 2006, pp. 75-84, ISSN 0253-5696.
8. Adriano, D. C. Trace elements in the terrestrial environment [en línea].
2.a ed., edit. Springer New York, 2001, 867 p., ISBN 978-1-4684-9505-8, DOI
http://dx.doi.org/10.1007/978-0-387-21510-5, [Consultado: 28 de noviembre
de 2015], Disponible en: <http://link.springer.com/pter/10.1007/978-0-387-21510-5_1>.
9. Sherameti, I. y Varma, A. Soil Heavy Metals [en línea]. (ser. Soil
Biology), vol. 19, edit. Springer Berlin Heidelberg, 2010, 477 p., ISBN 978-3-642-02435-1,
[Consultado: 28 de noviembre de 2015], Disponible en: <http://link.springer.com/pter/10.1007/978-3-642-02436-8_1>.
10. Sunderman, F. W. Elements and Their Compounds in the Environment [en línea].
(eds. Merian E., Anke M., Ihnat M., y Stoeppler M.), edit. Wiley-VCH Verlag
GmbH, 2004, ISBN 978-3-527-61963-4, DOI http://dx.doi.org/10.1002/9783527619634.ch34c,
[Consultado: 28 de noviembre de 2015], Disponible en: <http://onlinelibrary.wiley.com/doi/10.1002/9783527619634.ch34c/summary>.
11. Marmiroli, N. y Maestri, E. ‘‘Health Implications of Trace Elements in the
Environment and the Food Chain’’ [en línea]. En: ed. Prasad M. N. V.,
Trace Elements as Contaminants and Nutrients, edit. John Wiley & Sons, Inc.,
2008, pp. 23-53, ISBN 978-0-470-37012-4, DOI http://dx.doi.org/10.1002/9780470370124.ch2,
[Consultado: 28 de noviembre de 2015], Disponible en: <http://onlinelibrary.wiley.com/doi/10.1002/9780470370124.ch2/summary>.
12. Muñiz, U. O. Los microelementos en la agricultura [en línea].
edit. Agencia de Información y Comunicacion para la Agricultura (Agrinfor),
2008, 132 p., ISBN 978-959-246-201-4, [Consultado: 28 de noviembre de 2015],
Disponible en: <http://www.libreroonline.com/cuba/libros/7050/olegario-muniz-ugarte/los-microelementos-en-la-agricultura.html>.
13. Hernández, A.; Ascanio, M. O.; Morales, M. y Cabrera, A. ‘‘Correlación
de la Nueva Versión de Clasificación Genética de los Suelos
de Cuba, con clasificaciones internacionales (Soil Taxonomy y FAO-UNESCO) y
clasificaciones nacionales (2da Clasificación Genética y Clasificación
de series de suelos)’’. En: VI Congreso Nacional de la Ciencia del Suelo, edit.
Instituto de Suelos, Ministerio de la Agricultura y Sociedad Cubana de la Ciencia
del Suelo, La Habana, Cuba, 2006, p. 62, ISBN 959-7023-35-0.
14. Hernández, A.; Pérez, J.; Bosch, D. y Castro, N. Clasificación
de los suelos de Cuba 2015. edit. Ediciones INCA, Mayabeque, Cuba, 2015, 93
p., ISBN 978-959-7023-77-7.
15. Alvarez, J. R. E.; Montero, A. A.; Jiménez, N. H.; Muñiz,
U. O.; Padilla, A. R.; Molina, R. J. y Vera, S. Q. de. ‘‘Nuclear and related
analytical methods applied to the determination of Cr, Ni, Cu, Zn, Cd and Pb
in a red ferralitic soil and Sorghum samples’’. Journal of Radioanalytical
and Nuclear Chemistry, vol. 247, no. 3, marzo de 2001, pp. 479-486, ISSN
0236-5731, 1588-2780, DOI 10.1023/A:1010640009301.
16. CEADEN. Determinación de metales por espectrofotometría de
absorción atómica en suelo y abono orgánico. no. IA 6746:
11-1999, Inst. CEADEN, 2010, p. 6.
17. Muñiz, O.; Arozarena, N. y Grün, M. ‘‘Contenido de Cd, Pb, Cu,
Zn, Ni y Cr en los principales suelos cubanos’’. En: Resúmenes del 1er
Congreso de la Sociedad Cubana de la Ciencia del Suelo, La Habana, Cuba, 1988,
p. 224.
18. Muniz, O.; Arozarena, N.; Gonzalez, M. y Irigoyen, H. ‘‘Availability of
micronutrients in Cuban soils’’. Tagungsbericht - Akademie der Landwirtschaftswissenschaften
der Deutschen Demokratischen Republik, vol. 267, 1988, pp. 321-326, ISSN
0138-2659.
19. Camacho, E. y Paulín, J. R. ‘‘Génesis de un suelo ferralítico
Rojo con predominio de boehmita sobre caliza en la provincia Habana, Cuba’’.
Ciencias de la Agricultura, vol. 15, 1983, pp. 49–57, ISSN 0122-8420.
20. Ruiz, J. y Perez, J. J. M. ‘‘Algunas consideraciones sobre la formación
de los suelos rojos de la región de San Miguel de los Baños, Cuba’’.
Ciencias de la Agricultura, no. 18, 1984, pp. 81–89, ISSN 0122-8420.
21. Cárdenas, A.; Baisre, J. y Ortega, F. ‘‘El suelo ferritico púrpura
de Cuba’’. Ciencias de la Agricultura, no. 29, 1986, pp. 70-83, ISSN
0122-8420.
22. Lindsay, W. L. y Norvell, W. A. ‘‘Development of a DTPA Soil Test for Zinc,
Iron, Manganese, and Copper1’’. Soil Science Society of America Journal,
vol. 42, no. 3, 1978, p. 421, ISSN 0361-5995, DOI 10.2136/aj1978.03615995004200030009x.
23. Muñiz, O.; Molina, J.; Quicute, S. y Estevez, J. ‘‘Heavy metal pollution
in a rhodic ferralsol of Cuba’’ [en línea]. En: eds. Horst W. J., Schenk
M. K., Bürkert A., Claassen N., Flessa H., Frommer W. B., Goldbach H.,
Olfs H.-W., Römheld V., Sattelmacher B., Schmidhalter U., Schubert S.,
Wirén N. v, y Wittenmayer L., Plant Nutrition, edit. Springer Netherlands,
2001, pp. 994-995, ISBN 978-0-7923-7105-2, [Consultado: 28 de noviembre
de 2015], Disponible en: <http://link.springer.com/chapter/10.1007/0-306-47624-X_484>.
24. Muñiz, O.; Estévez, J.; Quicute, S.; Montero, A.; Fraser,
T. y Vega, E. ‘‘Extracción de Ni y Cd por la patata cultivada sobre suelo
Ferralítico Rojo de la provincia Habana’’. En: Fernández J., Nogales
R., y Romero E., ed. Gallardo L. J. F., Medioambiente en Iberoamérica.
Visión desde la física y química en los albores del Siglo
XXI, edit. Graficas Diputación de Badajoz, España, 2006, pp. 261-266,
ISBN 978-84-611-0352-2.
25. Grün, M.; Machelett, B. y Podlesak, W. ‘‘Heavy metal limiting values
in soils based on the extraction with boiling 1.5 N nitric acid’’. En: eds.
Welte E. y Szabolas I., Proceedings of the 4th International CIEC Symposium,
edit. Fed. Rep. of Germany, Germany, 1987, pp. 401-408.
26. CODEX. Norma General del CODEX para los contaminantes y las toxinas presentes
en los alimentos. no. Codex Stan 193-1995, Inst. CODEX, 2007, p. 50.
27. Selim, H. M. Dynamics and Bioavailability of Heavy Metals in the Rootzone.
edit. CRC Press, 15 de marzo de 2011, 308 p., ISBN 978-1-4398-2623-2.
28. Adriano, D. C. Biogeochemistry of trace metals. edit. Lewis Publishers,
16 de junio de 1992, 536 p., ISBN 978-0-87371-523-2.
29. Reimann, C. y Caritat, P. de. Chemical Elements in the Environment [en línea].
edit. Springer Berlin Heidelberg, 1998, 398 p., ISBN 978-3-642-72018-5, http://dx.doi.org/10.1007/978-3-642-72016-1,
[Consultado: 28 de noviembre de 2015], Disponible en: <http://link.springer.com/pter/10.1007/978-3-642-72016-1_1>.
30. Wasserman, M. A.; Bartoly, F.; Poquet, I. y Perez, D. V. ‘‘Assessment of
the mobility and bioavailability of 60Co and 137Cs in contaminated soils’’ [en
línea]. En: Proceedings of the 5. Regional congress on radiation protection
and safety; 2. Iberian and Latin American Congress on Radiological Protection
Societies; Regional IRPA Congress, edit. Sociedade Brasileira de Protecao Radiologica,
Recife, PE (Brazil); International Radiation Protection Association (IRPA),
Washington, DC (United States), Brasil, 2001, p. 1776, [Consultado: 28
de noviembre de 2015], Disponible en: <https://inis.iaea.org/search/search.aspx?orig_q=RN:33034452>.
31. Rékási, M. y Filep, T. ‘‘Fractions and background concentrations
of potentially toxic elements in Hungarian surface soils’’. Environmental
Monitoring and Assessment, vol. 184, no. 12, 21 de febrero de 2012, pp.
7461-7471, ISSN 0167-6369, 1573-2959, DOI 10.1007/s10661-011-2513-9.
32. Chaney, R. L.; Malik, M.; Li, Y. M.; Brown, S. L.; Brewer, E. P.; Angle,
J. S. y Baker, A. J. ‘‘Phytoremediation of soil metals’’. Current Opinion
in Biotechnology, vol. 8, no. 3, junio de 1997, pp. 279-284, ISSN 0958-1669,
DOI 10.1016/S0958-1669(97)80004-3.
33. Yang, X.; Feng, Y.; He, Z. y Stoffella, P. J. ‘‘Molecular mechanisms of
heavy metal hyperaccumulation and phytoremediation’’. Journal of Trace Elements
in Medicine and Biology, vol. 18, no. 4, 27 de junio de 2005, pp. 339-353,
ISSN 0946-672X, DOI 10.1016/j.jtemb.2005.02.007.
34. Galardi, F.; Corrales, I.; Mengoni, A.; Pucci, S.; Barletti, L.; Barzanti,
R.; Arnetoli, M.; Gabbrielli, R. y Gonnelli, C. ‘‘Intra-specific differences
in nickel tolerance and accumulation in the Ni-hyperaccumulator Alyssum
bertolonii’’. Environmental and Experimental Botany, vol. 60,
no. 3, julio de 2007, pp. 377-384, ISSN 0098-8472, DOI 10.1016/j.envexpbot.2006.12.011.
35. Berazaín, I. R. ‘‘Estudios en plantas acumuladoras e hiperacumuladoras
de níquel en las serpentinas del Caribe’’. Revista del Jardín
Botánico Nacional, vol. 20, 1999, pp. 17-30, ISSN 0253-5696.
36. Berazain, I. R. ‘‘The influence of ultramafic soils on plants in Cuba’’.
South African Journal of Science, vol. 97, no. 11-12, 2001, pp. 510-512,
ISSN 0038-2353, 0038-2353.
37. Berazaín, R.; Fuente, V. de la; Sánchez-Mata, D.; Rufo, L.;
Rodríguez, N. y Amils, R. ‘‘Nickel localization on tissues of hyperaccumulator
species of Phyllanthus L. (euphorbiaceae) from Ultramafic Areas of Cuba’’. Biological
Trace Element Research, vol. 115, no. 1, 2007, pp. 67-86, ISSN 0163-4984,
1559-0720, DOI 10.1385/BTER:115:1:67.
38. Martínez, C. M.; Lestón, M. G.; Castro, C. B. y Kidd, P. ‘‘Aplicación
de plantas hiperacumuladoras de níquel en la fitoextracción natural:
el género Alyssum L.’’. Ecosistemas: Revista científica
y técnica de ecología y medio ambiente, vol. 16, no. 2, 2007,
pp. 26-43, ISSN 1697-2473.
39. Marrero, C. J.; Amores, S. I. y Coto, P. O. ‘‘Fitorremediación, una
tecnología que involucra a plantas y microorganismos en el saneamiento
ambiental’’. ICIDCA. Sobre los Derivados de la Caña de Azúcar,
vol. 46, no. 3, 2012, pp. 52–61, ISSN 0138-620, 1025-3076.
40. Plant-Based Remediation Processes [en línea]. (ed. Gupta D. K.),
(ser. Soil Biology), vol. 35, edit. Springer Berlin Heidelberg, Berlin, Heidelberg,
2013, 299 p., ISBN 978-3-642-35563-9, DOI http://dx.doi.org/10.1007/978-3-642-35564-6,
[Consultado: 28 de noviembre de 2015], Disponible en: <http://link.springer.com/10.1007/978-3-642-35564-6>.
41. Meuser, H. Soil Remediation and Rehabilitation [en línea]. (ser.
Environmental Pollution), vol. 23, edit. Springer Netherlands, Dordrecht, 2013,
406 p., ISBN 978-94-007-5750-9, DOI http://dx.doi.org/10.1007/978-94-007-5751-6,
[Consultado: 28 de noviembre de 2015], Disponible en: <http://link.springer.com/10.1007/978-94-007-5751-6>.
42. Treto, E.; García, M.; Viera, R. M. y Febles, J. M. ‘‘Advances in
organic soil management.’’. En: Sustainable agriculture and resistance: transforming
food production in Cuba, edit. ACTAF, Cuba, 2002, pp. 164-189, ISBN 0-935028-87-0,
CABDirect2.
43. Berc, J.; Muñiz, O. y Calero, B. ‘‘Vermiculture Offers A New Agricultural
Paradigm’’. BioCycle, vol. 45, no. 6, 2004, pp. 56-57, ISSN 0276-5055.
44. Rodríguez, A. M.; Muñiz, U. O.; Calero, M. B.; Martínez,
R. F.; Montero, Á. A.; Limeres, J. T.; Orphee, M. M. y Aguilar, A. A.
M. de. ‘‘Contenido de metales pesados en abonos orgánicos, sustratos
y plantas cultivadas en organopónicos’’. Cultivos Tropicales,
vol. 33, no. 2, junio de 2012, pp. 05-12, ISSN 0258-5936.
45. da Silva, A. C. M. A.; Marker, A.; Figueirinha, F. R. F. R. y da Silva,
F. A. N. Guia para avaliação do potencial de contaminação
em imóveis. edit. Companhia de Tecnologia de Saneamento Ambiental, São
Paulo, Brasil, 2003, 80 p., ISBN 85-86624-25-X.
46. Swartjes, F. A.; Rutgers, M.; Lijzen, J. P. A.; Janssen, P. J. C. M.; Otte,
P. F.; Wintersen, A.; Brand, E. y Posthuma, L. ‘‘State of the art of contaminated
site management in The Netherlands: Policy framework and risk assessment tools’’.
Science of The Total Environment, vol. 427-428, 15 de junio de 2012,
pp. 1-10, ISSN 0048-9697, DOI 10.1016/j.scitotenv.2012.02.078.
Recibido: 2 de
septiembre de 2014
Aceptado: 8 de agosto de 2015
Dr.C. Olegario
Muñiz Ugarte, Instituto de Suelos, Autopista Costa-Costa,
km 8½, Apdo. 8022, CP 10 800, Capdevila, Boyeros, La Habana. Email: olemuniz@ceniai.inf.cu





